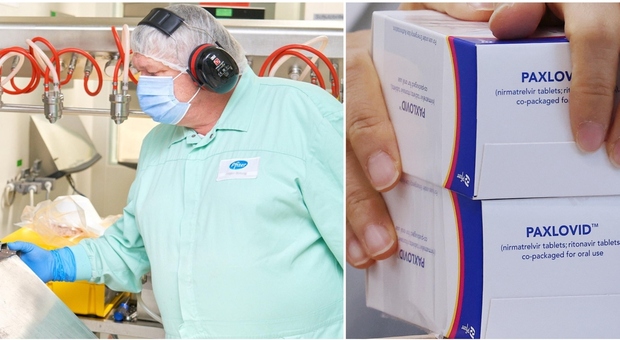
Arriva sul mercato europeo un altro, nuovo, farmaco per trattare la malattia Covid-19 nei primi giorni. È efficace contro Omicron e altre varianti ed è sviluppato per l'uso a casa. L'Agenzia europea del farmaco Ema ha dato il via libera a questo antivirale e ne raccomanda l'autorizzazione all'immissione in commercio condizionata. Si tratta del medicinale Paxlovid: è un farmaco anti-Covid (è una pillola) che si prende per via orale prodotto da Pfizer. Si tratta di una notizia molto importante perché i precedenti farmaci sono efficaci ma in misura ridotta (la pillola Merck - molnupiravir - si ferma a un 30% di efficacia) rispetto ai principi attivi di queste compresse sviluppate da Pfizer. Questo antivirale, infatti, può fare la differenza. Lo dice la numero uno della Sanità della Commissione europea Stella Kyriakides. Paxlovid «ha il potenziale per fare davvero la differenza per le persone ad alto rischio di progressione verso il Covid grave». Così la commissaria Ue alla Salute Stella Kyriakides dopo l'ok dell'Ema al farmaco. «Con l'autorizzazione di Paxlovid questa settimana sono 6 i farmaci contro il Covid-19 autorizzati nell'ambito della strategia terapeutica Ue e - aggiunge - altri arriveranno nelle prossime settimane». La pillola di Pfizer «è il primo antivirale orale per uso domestico nel nostro portafoglio e abbiamo visto prove promettenti della sua efficacia contro Omicron e altre varianti».
«Abbiamo il vaccino che è fondamentale. E ora questo nuovo farmaco che, però, non sostituisce il vaccino ma va bene nei primi giorni di infezione per chi ha scarse risposte immunitarie e fattori di rischio, come accade con i monoclonali», dice Silvio Garattini, fondatore e presidente dell'Istituto di ricerche farmacologiche Mario Negri Irccs. «Aspettiamo che ci siano dei farmaci - conclude - che agiscono di più sulla malattia. C'è da sperare perché in tutto il mondo ci sono moltissimi laboratori che stanno lavorando, sia per fare nuovi medicinali contro la malattia in atto, sia per mettere a punto nuovi vaccini che coprano molte più varianti rispetto a quelle coperte dai vaccini disponibili. C'è ancora molto lavoro da fare per avere una terapia. Così come abbiamo un antibiotico quando dobbiamo curare una polmonite, dovremmo avere un farmaco ad attività antivirale quando è in corso il Covid, in grado di impedire alla malattia di progredire», ha aggiunto.
Ecco cosa scrive nel suo comunicato l'agenzia Ema: «Il comitato per i medicinali per uso umano dell'EMA (CHMP) ha raccomandato di autorizzare Paxlovid per il trattamento della COVID-19 negli adulti che non richiedono ossigeno supplementare e che sono a maggior rischio che la malattia diventi grave. Paxlovid è il primo farmaco antivirale da somministrare per bocca raccomandato nell'UE per il trattamento della COVID-19».
Come funziona la pillola sviluppata da Pfizer? Lo abbiamo spiegato qui.
La valutazione dell'agenzia europea del farmaco
L'Ema ha valutato i dati di uno studio che ha coinvolto pazienti con Covid-19 mostrando che il trattamento con Paxlovid ha ridotto significativamente le ospedalizzazioni o i decessi nei pazienti che hanno almeno una condizione sottostante che li mette a rischio di COVID-19 grave. L'analisi è stata fatta in pazienti che hanno ricevuto Paxlovid o placebo (trattamento fittizio) entro 5 giorni dall'inizio dei sintomi di Covid-19 e che non hanno ricevuto, né si attendevano di ricevere, un trattamento con anticorpi.
Nel mese successivo al trattamento, lo 0,8% (8 su 1.039) dei pazienti che hanno ricevuto Paxlovid sono stati ricoverati per più di 24 ore, rispetto al 6,3% (66 su 1.046) di quelli che hanno ricevuto il placebo. Non ci sono stati decessi nel gruppo Paxlovid mentre ce ne sono stati 12 nel gruppo placebo. «I dati degli studi clinici presentati dall'azienda nella domanda di autorizzazione all'immissione in commercio saranno pubblicati sul sito web dei dati clinici dell'Agenzia a tempo debito», si legge.
La maggior parte dei pazienti nello studio sono stati infettati con la variante Delta. «Sulla base degli studi di laboratorio, ci si aspetta che Paxlovid sia attivo anche contro Omicron e altre varianti», si legge nel comunicato.
L'analisi europea sulla sicurezza
«Il profilo di sicurezza di Paxlovid era favorevole e gli effetti collaterali erano generalmente lievi», scrive Ema. Paxlovid è composto da due differenti compresse che contengono due diversi principi attivi: il nirmatrelvir e il ritonavir. Il ritonavir, scrive Ema, è noto per influenzare l'azione di molti altri farmaci, e avvertimenti e consigli sono stati inclusi nelle informazioni sul prodotto di Paxlovid da parte di Pfizer.
L'interazione con i contraccettivi
In un documento diffuso dalla multinazionale si evidenzia l'importanza di avvertire medico e farmacista prima di assumere Paxlovid. Bisogna comunicare ad esempio se si hanno delle allergie, se si soffre di una malattia epatica o renale, se donna se si è incinta o si sta pianificando una gravidanza o si sta allattando un bambino e se si ha qualsiasi malattia grave. Bisogna anche comunicare se si sta prendendo un contraccettivo ormonale combinato.
Quali sono i contraccettivi ormonali combinati? Sono la pillola, il cerotto o l'anello. Contengono due ormoni: un estrogeno ed un progestinico. «Paxlovid può influenzare il funzionamento della pillola anticoncezionale», avverte in un documento Pfizer. «Le donne devono usare un'altra forma di contraccezione alternativa efficace o un ulteriore metodo contraccettivo di barriera», sottolinea lo stesso documento.
Un aspetto su cui prestare attenzione, secondo Giuseppe Remuzzi, direttore dell'Istituto di ricerche farmacologiche Mario Negri Irccs. «Paxlovid non può essere usato insieme ad altri medicinali e quindi bisogna valutare il rischio di interazioni importanti che possono esserci. E poi va tenuto presente che è controindicato in pazienti con grave insufficienza renale o epatica. Al contrario del vaccino, inoltre, Paxlovid non va dato in gravidanza e alle donne che non usano contraccettivi», ha detto Remuzzi.
L'agenzia Ema ha ritenuto nella sue conclusioni che i benefici del farmaco sono maggiori dei suoi rischi e ora invierà le sue raccomandazioni alla Commissione europea per una decisione rapida applicabile in tutti gli Stati membri dell'UE.
Oggi viene approvata l'autorizzazione all'immissione in commercio condizionata. Che vuol dire? È una formula usata come procedura di autorizzazione rapida per accelerare l'approvazione di medicinali durante un'emergenza. Questo tipo di autorizzazioni permettono il via libera di «farmaci che soddisfano un bisogno medico insoddisfatto sulla base di dati meno completi di quelli normalmente richiesti», si legge. Perché? «Questo accade se il beneficio della disponibilità immediata di un farmaco per i pazienti supera il rischio inerente al fatto che non tutti i dati sono ancora disponibili. L'autorizzazione condizionata garantisce che il medicinale approvato soddisfi i rigorosi standard UE di efficacia, sicurezza e qualità e che sia prodotto in strutture approvate e certificate, in linea con gli elevati standard farmaceutici per la produzione su larga scala. Una volta che un'autorizzazione al commercio condizionata è concessa, le aziende devono fornire ulteriori dati entro scadenze predefinite per confermare che i benefici continuano a superare i rischi. Per Paxlovid l'azienda che commercializza il farmaco fornirà ulteriori dati per rafforzare la garanzia sulla qualità farmaceutica del farmaco», spiega ancora l'Ema nel suo comunicato.
La pillola Merck
In Italia, è già disponibile anche l'antivirale orale della Msd (Merck) - la pillola Lagevrio, con la quale sono stati già trattati 1.662 pazienti - dopo che lo scorso novembre l'Ema aveva emesso un parere per supportare le autorità nazionali che avessero deciso su un possibile uso precoce delle capsule prima dell'autorizzazione all'immissione in commercio.
I monoclonali
La variante Omicron non è contrastata dagli anticorpi monoclonali, invece. Dopo lo stop della Fda statunitense ai due monoclonali di Eli Lilly e Regeneron perchè poco efficaci contro la variante, ora, per la stessa ragione, arriva una frenata anche per gli anticorpi monoclonali in studio in Italia. Toscana Life Sciences sviluppo ha infatti annunciato di aver sospeso temporaneamente l'arruolamento di nuovi pazienti positivi al Covid nell'ambito della sperimentazione clinica di fase II/III in corso su MAD0004J08, l'anticorpo monoclonale individuato dal team di ricerca della Fondazione Tls coordinato dal professor Rino Rappuoli. I dati in vitro su Omicron, si spiega, «rilevano una perdita di efficacia» del farmaco.